Kamagra gibt es auch als Kautabletten, die sich schneller auflösen als normale Pillen. Manche Patienten empfinden das als angenehmer. Wer sich informieren will, findet Hinweise unter kamagra kautabletten.
Lettre n 4 cm (psp) pour site public jpc 27.12.2012

ACADÉMIE NATIONALE DE PHARMACIE
SANTÉ PUBLIQUE - MÉDICAMENT - PRODUITS DE SANTÉ - BIOLOGIE - SANTÉ ET ENVIRONNEMENT
Fondée le 3 août 1803 sous le nom de Société de Pharmacie de Paris
Reconnue d'utilité publique le 5 octobre 1877
VEILLE SCIENTIFIQUE
LETTRE n° 4
éditée sous l'égide de la Commission Prospective scientifique et Programmation
Ce document résulte d'une veille prospective de l'Académie nationale de Pharmacie réalisée périodiquement dans le domaine de la santé et de l'innovation thérapeutique ainsi que dans le domaine de l'environnement/santé. Elle cherche également à mettre en relief les start-up ou Biotechs impliquées dans ces mêmes domaines.
Pour faciliter la lecture, les informations sont signalées par des lettres : F pour recherche fondamentale ; P pour recherche préclinique ; C pour recherche clinique.
SOMMAIRE
Des regroupements pharmaceutiques en faveur de l'innovation
Innovation thérapeutique
1. Une première thérapie génique en Europe (C)
2. Folforinox : un traitement plus efficace du cancer du pancréas (C)
3. Échec des vaccins anti-Alzheimer ? (C)
4. Des biothérapeutiques à partir d'acides aminés non naturels (F)
5. Des virus pour guérir les cancers, les virus oncolytiques (P)
6. Moteurs moléculaires (F)
7. Une nouvelle génération d'inhibiteur du protéasome, le Kyprolis® (C)
8. L'inhibition de EPHA4 pour le traitement de la maladie de Charcot (P)
9. Vers un traitement des myopathies par des inhibiteurs de phosphodiestérases ?(C)
Biotechs dans le domaine de la Santé
GENEFIT / EFFIMUNE / IMMUNID / STAGO
Acad nat Pharm / Lettre n° 4 déc-2012
DES REGROUPEMENTS PHARMACEUTIQUES EN FAVEUR DE L'INNOVATION
1. Dix laboratoires pharmaceutiques (Abbott, AstraZeneca, Boehinger Ingelheim, Bristol-Myers Squibb, Eli Lilly,
GlaxoSmithKline, Johnson & Johnson, Pfizer, Genentech membre du groupe Roche, et Sanofi) ont annoncé le
19 septembre 2012 la création de « TransCelerate Biopharma Inc (TransCelerate) », le plus grand groupement
existant pour identifier et résoudre les challenges du développement de médicaments avec comme finalité
améliorer la qualité des études cliniques et mettre plus rapidement de nouveaux médicaments à la disposition
2. Parallèlement les laboratoires pharmaceutiques, Janssen Research & Development, LLC (Janssen R&D), Merck
and Eli Lilly ont annoncé le 15 novembre 2012 l'établissement d'une banque de données communes afin
d'améliorer l'efficacité des essais cliniques sponsorisés par l'industrie. Celle-ci renfermera des informations clés
en ce qui concerne les sites d'essais cliniques comme l'infrastructure et les bonnes pratiques cliniques de façon
à gagner du temps et minimiser des tâches administratives souvent redondantes.
Ces banques de données n'incluront aucunes données concernant les patients.
INNOVATIONS THÉRAPEUTIQUES
1. Une première thérapie génique en Europe
Après deux ans et demi de réponses négatives, le Comité des médicaments à usage humain (CHMP) de
l'European Medicines Agency (EMA) a finalement approuvé le Glybera ou alipogene tiparvovec, pour le
traitement des patients souffrant de déficience génétique en lipoprotéine lipase (LPL), associé à de sévères et
multiples pancréatites pour laquelle il n'existe actuellement aucune autre alternative.
Le gène LPL normal et fonctionnel est délivré par un vecteur dérivé d'un adénovirus associé (AAV) de sérotype
21 qui a une propension naturelle à se diriger vers les cellules musculaires. Glybera est administré au travers de
petites injections intramusculaires dans les jambes.
Un certain nombre d'autres approches de thérapie génique sont actuellement en développement ciblant d'autres
organes comme la rétine, le foie ou encore le cerveau. Le feu vert donné à Glybera devrait booster les
recherches en ce domaine en dépit de barrières, comme la complexité du traitement, mais aussi des questions
sociales et éthiques.
Source : Nature Reviews Drug Discovery 11, 664 (September 2012)
2. Folforinox : un traitement plus efficace du cancer du pancréas
Ce protocole (trois essais positifs) consiste en l'administration conjointe de quatre molécules que sont
l'oxaliplatine, l'irinotecan, le 5-fluorouracile et l'acide folinique. Des réponses objectives ont été obtenues chez
plus de 30 % des patients et l'augmentation de survie constatée était de plus de quatre mois, comparativement
au traitement standard, la gemcitabine. On retiendra également l'arrivée du panitumumab dans l'arsenal
thérapeutique des tumeurs colorectales avancées, en première ligne en association avec le FOLFOX et en
deuxième ligne en association avec le FOLFIRI. Enfin, un nouvel antiangiogénique, l'aflibercept (VEGF-trap),
fait son entrée parmi les médicaments dont il faudra tenir compte à l'avenir dans la stratégie thérapeutique des
cancers colorectaux métastatiques.
L'adénome du pancréas était la 4ème cause de mortalité tous cancers confondus aux USA en 2010, le pronostic
vital à cinq ans étant de 6 % en Europe et aux États-Unis …
Source : Conroy T., Desseigne F., Ychou M., et al. FOLFIRINOX versus gemcitabine for metastatic pancreatic cancer
N Engl J Med 2011; 364:1817-1825
Acad nat Pharm / Lettre n° 4 déc-2012
3. Échec des vaccins anti-Alzheimer ?
Plusieurs vaccins de type immunisation passive, basés sur des anticorps ciblant les « peptides β-amyloïdes »,
sont en cours d'essais, cliniques. Les essais de phase III du bapineuzupab, co-devéloppé actuellement par
Pfizer et Johnson and Johnson (antérieurement par Elan & Wyeth), se sont révélés très décevants1. Aussi en août
2012, les deux groupes ont décidé de suspendre toute formulation intraveineuse de ce vaccin. Si le programme
bapineuzumab IV est mort, l'étude en phase II (moins avancée) d'une version sous-cutanée du traitement se
En revanche, le solanezumab (phase II) développé par Lilly, diminuerait la vitesse du déclin cognitif et de la
perte de la mémoire d'environ 30 % chez les patients traités aux premiers stades de la maladie2.
L'essai de phase II du gantenerumab a montré une diminution dose-dépendante des niveaux d'amyloïde dans
plusieurs régions cérébrales des malades (différences moyennes pour la région corticale - 15,6 % par rapport au
placebo (dose de 60 mg), et - 35,7 % (à 200 mg)3. Le mécanisme suggéré est une augmentation de la
phagocytose de Aβ (mécanisme qui permet à certaines cellules spécialisées d'absorber et de détruire des
particules étrangères). Un essai de phase II est actuellement en cours, chez des patients en phase précoce de la maladie d'Alzheimer.
Du côté de l'immunisation active, deux vaccins sont en cours d'essais, le ACC-001 et le CAD106.
Les résultats d'un essai clinique de phase 1 du CAD106 développé par une équipe suédoise du Karolinska
Institute contre la maladie d'Alzheimer, viennent d'être publiés dans The Lancet Neurology4. Ce vaccin
CAD106 a été testé sous deux dosages, en double aveugle contre placebo, sur un total de 58 patients au stade 1
(léger) et 2 (modéré) de la maladie, entre 50 et 80 ans. Une réponse immunitaire a été constatée chez 82 % des
patients ayant reçu le dosage le plus élevé. Aucune réaction sévère n'a été enregistrée au cours des trois ans de
suivi médical. Qu'en sera-t-il de son efficacité thérapeutique ?
ACC-001 est un fragment de Aβ(1-6) relié à une protéine transporteuse et à une saponine comme adjuvant. Un
essai clinique II, multicentrique, randomisé, triple aveugle contrôlé versus placebo, doit démarrer fin 2012
incluant des patients souffrant d'Alzheimer de façon modérée.
Sources :
1. Delrieu J., Ousset P.-J., Caillaud C., Vellas B., Clinical trials in Alzheimer's disease: immunotherapy approaches
J Neurochem. 2012 Jan; 120 Suppl 1:186-93
2. Farlow M, et al. Safety and biomarker effects of solanezumab in patients with Alzheimer's disease
Alzheimers Dement 2012 Jul; 8 (4):261-71
3. Ostrowitzki S et al., Mechanism of Amyloid Removal in Patients With Alzheimer Disease Treated With
Gantenerumab, Arch Neurol. 2012; 69 (2):198-207
4. Wimblad B et al., Safety, tolerability, and antibody response of active Aβ immunotherapy with CAD106 in patients
with Alzheimer's disease: randomised, double-blind, placebo-controlled, first-in-human study. Lancet Neurol. 2012; 11 (7): 597-604
5. Delrieu et al., Clinical trials in Alzheimer's disease: immunotherapy approaches
Neurochem. 2012; 120 Suppl 1: 186-93 (Revue)
Différentes approches en cours de développement :
Solanezumab (Lilly)
Immunisation passive
Bapineuzumab (Elan Wyeth)
Ponezumab (Pfizer)
Phase III (arrêté)
Ganteneruzumab (Roche)
Phase II (pro AD)
Intravenous immunoglobulin (Baxter)
Active immunisation
ACC-001 (Elan Wyeth)
CAD-106 (Novartis)
Acad nat Pharm / Lettre n° 4 déc-2012
INHIBITEURS de SECRETASE
Semagacestat (Lilly)
Phase III (negative)
Inhibiteur de Gamma secretase
Inhibiteurs de Beta secretase
Phase II (pro/early AD)
AGENTS ANTI-
Tramiprosate (Neurochem)
Phase II (negative)
AGGREGANTS
Curcumin (John Douglas)
Phase III (planned)
4. Des biothérapeutiques à partir d'acides aminés non naturels
Relier de petites molécules à des protéines est une pratique établie dans l'industrie pharmaceutique. C'est en
particulier le cas des anticorps monoclonaux liés à des cytotoxiques comme le trastuzumab (ou Herceptine)-
DM1 de Genentech ou le Mylotarg (gemtuzumab-ozogamycin) volontairement retiré du marché en juin dernier
Toutefois, les 20 acides aminés naturels ne permettant pas de modifications à l'infini, deux biotech se sont
tournés vers l'élaboration de médicaments renfermant des acides aminés non naturels.
Ainsi Ambrx, basée à La Jolla en Californie, développe une hormone modifiée du nom de ARX201 comme
facteur de croissance à longue durée d'action avec une administration une fois par mois. L'hormone de
croissance1 est liée à une chaîne polyéthylène glycol par l'intermédiaire d'un cycle aromatique.
L'étude de phase II de ce composé, développé en collaboration avec Serono, a fait l'objet d'une communication
en mai 2011. IL est actuellement en essais de phase III.
De son côté Allozyne, basée à Seattle, développe également un médicament incluant des acides aminés non
naturels, l'AZ01 pour le traitement longue durée des scléroses multiples. L'interféron β est lié à une double chaîne polyéthylène glycol par la chimie dite de « click chemistry ».
Pour inclure des acides aminés non naturels dans ces deux protéines, hormone de croissance et interféron
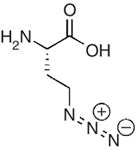
pégylés, les procédés font appel à E. coli. Ainsi, dans le cas d'AZ01 une azido-homoalanine est introduite dans
le milieu de culture à la place de la méthionine. Cette azido-homoalanine est suffisamment ressemblante (leurre)
à la méthionine pour que la bactérie l'incorpore dans la séquence protéinique2. La phase 1a a été complétée en
janvier 2011et la phase 1b en octobre de la même année.
Méthionine Azido-homoalanine
Sources : 1. Cho H. et al., Optimized clinical performance of growth hormone with an expanded genetic code
PNAS 2011; 108 (22): 9060-5
2. Naim N.-W. et al., Development of Copper-Catalyzed Azide-Alkyne Cycloaddition for Increased in Vivo
Efficacy of Interferon β-1b by Site-Specific PEGylation, Bioconj Chem. 2012; 23 (10): 2087-97
5. Des virus pour guérir les cancers, les virus oncolytiques
Jusqu'à une époque récente on pensait que les virus oncolytiques exerçaient leur activité seulement en se
répliquant avec les cellules cancéreuses puis en les détruisant. Il semblerait aujourd'hui que, au-delà de détruire
les cellules cancéreuses, ils stimuleraient le système immunitaire. En quelque sorte, les virus oncolytiques
agiraient comme des vaccins anti-cancer.
Acad nat Pharm / Lettre n° 4 déc-2012
Leur efficacité est telle que divers laboratoires développent actuellement de tels virus, comme indiqué ci-après :
Nom de code
Étape développement
Type de virus
GLK-ONC1
Cincinnati Children Hospital
Seneca Valley Virus
Jennerex/Transgene
Parvorix
Reolysin
Oncolytics Biotech
Shanghai Sunway Biotech
Phase III (China)
Shanghai Sunway Biotech
Approved (China)
Le cas du Virus JX594/TG6006
Les laboratoires partenaires Transgene et Jennerex, ont annoncé que leur virus oncolytique JX594/TG6006 pour
le traitement de patients atteints de cancer du foie avancé a permis de doubler la survie chez les patients ayant
reçu une dose élevée vs une dose faible. Ces résultats d'essai clinique de phase II, porteurs d'espoir, ont été
présentés à la 62ème réunion annuelle de l'Association américaine pour l'étude des maladies du foie (American
Association for the Study of Liver Diseases, AASLD) à San Francisco.
Cet essai de phase II a été mené sur 30 patients recrutés aux États-Unis, au Canada et en Corée du Sud. Les
patients ayant reçu une dose élevée ont eu un bénéfice clinique statistiquement significatif en termes de survie
globale par rapport à ceux du groupe ayant reçu la dose faible. Le risque de décès des patients ayant reçu la dose
élevée de JX594/TG6006 s'avère réduit de près de 60 %. La survie moyenne avec dose élevée s'élève à 13,8
mois vs 6,7 mois avec une faible dose. C'est à la fois la preuve de la faisabilité d'une administration par voie
intra-veineuse d'un virus oncolytique mais aussi de son activité anti-tumorale et enfin de la sécurité de ce
nouveau composé, JX594/TG6006, chez des patients atteints de cancers du foie réfractaires au traitement par
6. Moteurs moléculaires
Des travaux novateurs menés par Nicolas GIUSEPPONE, professeur à l'Université de Strasbourg, et impliquant
des chercheurs du Laboratoire de matière et systèmes complexes (CNRS/Université Paris Diderot), valident
expérimentalement une approche biomimétique conceptualisée depuis plusieurs années dans le domaine des
En assemblant des milliers de molécules qui peuvent s'allonger ou se contracter, ces chimistes ont créé un
polymère qui reproduit le mouvement de l'unité de base d'un tissu musculaire. Pour que ces mouvements
minuscules se traduisent à notre échelle, de manière perceptible et utilisable ces chercheurs de l'université de
Strasbourg (Institut Charles SADRON) ont trouvé une solution, en mettant bout-à-bout des milliers de machines
moléculaires, pour former un polymère, afin que leurs mouvements synchronisés et cumulés finissent par
donner une contraction d'environ un micromètre, du même ordre que la longueur de contraction des sarcomères
qui constituent les myofibrilles, unité contractile de nos muscles.
Acad nat Pharm / Lettre n° 4 déc-2012
Pour imiter ainsi le processus de base de la contraction musculaire, les chimistes sont partis d'une classe de
machines moléculaires qu'on appelle des rotaxanes : une molécule constituée de cycles qui coulisse sur une
chaîne d'atomes, et change ainsi de longueur.
Il s'agit là d'une première avancée vers de futures micro-machines et micro-robots biomimétiques.
Source : Du G., Moulin E., Jouault N., Buhler E., Giuseppone N., Muscle-like Supramolecular Polymers: Integrated
Motion from Thousands of Molecular Machines Angewandte Chemie International Edition 2012 ; 47 (12): 2235-9
7. Une nouvelle génération d'inhibiteur du protéasome : le Kyprolis®
La FDA a approuvé en juillet dernier le carbilzomib ou Kyprolis® pour le traitement du myélome multiple. Il
s‘agit du second inhibiteur du protéasome mis sur le marché après le bortezomib ou Velcade®. Le traitement du
myélome multiple dispose désormais de ces deux molécules mais aussi d'immunomodulateurs comme le
thalidomide (2006), le lenalidomide ou Revlid® et du ponalidomide (phase III).
8. L'inhibition de EPHA4 pour le traitement de la maladie de Charcot
La sclérose latérale amyotrophique (SLA), également appelée maladie de Charcot, est une maladie
neurodégénérative des motoneurones de l'adulte. Elle correspond à l'atteinte des neurones moteurs situés dans la
corne antérieure de la moelle et les noyaux moteurs des derniers nerfs crâniens. L'incidence en France est d'un
nouveau cas survenant chaque année pour 100 000 habitants.
Une étude publiée dans Nature Medicine1 a montré que le récepteur 4 de l'éphrine type A contrôle la
dégénérescence motrice et la progression de la maladie, suggérant ainsi que l'inhibition de EPHA4 pourrait
représenter une stratégie thérapeutique. De petites molécules bloquant la liaison de l'éphrine à son récepteur A4
ont déjà été rapportée2.
Sources : 1. Van Hoecke A. et al., EPHA4 is a disease modifier of amyotrophic lateral sclerosis in animal models and in
humans, Nature Med. 2012; 18: 1418-1422
2. Noberini R., Koolpe M., Peddibhotla S., Dahl R., Su Y. et al., Small Molecules Can Selectively Inhibit
Ephrin Binding to the EphA4 and EphA2 Receptors, J Biol Chem. 2008 October 24; 283 (43): 29461-29472
9. Vers un traitement des myopathies par des inhibiteurs de phosphodiestérases
Une étude anglo-saxonne randomisée versus placebo portant sur neuf patients atteints de la maladie
dystrophique de Becker, caractérisée par la dégénérescence de la fibre musculaire striée aboutissant à une
atrophie progressive de la plupart des muscles dont la conséquence est un handicap moteur, a montré que le
tadalafil, un inhibiteur de phosphodiestérase V (cf Viagra) était susceptible, en boostant la NO-Cyclic guanosine
monophosphate (cGMP), de restaurer l'arrivée normale du sang dans les muscles de ces patients levant ainsi
Pourquoi un tel traitement ? On connait le rôle de l'oxyde nitrique synthase neuronale, une protéine
enzymatique qui synthétise l'oxyde nitrique, un radical libre présent dans la circulation sanguine. Cette NO
synthase est associée par le biais de la dystrophine au sous- domaine cytosolique de la dystrophine dans le
muscle squelettique. Toute libération de NO provoque le relâchement des muscles lisses et une augmentation
locale du flux sanguin. Quand un muscle sain est sujet à un exercice, NO atténue la vasoconstriction
adrénergique optimisant ainsi la perfusion du muscle. C'est ce mécanisme qui, selon les auteurs, serait
défectueux chez ces patients, d'où l'idée de booster la NO-cGMP pour produire NO.
Source : Elizabeth A. Martin, et al., Tadalafil Alleviates Muscle Ischemia in Patients with Becker Muscular Dystrophy
Sciences Translational Medicine 2012; 4 (162): 162ra155
10. Divers
R. Duffy et al., Discovery of anticancer drugs from antimalarial natural products: a MEDLINE literature review Drug Discovery Today 2012; 17 (17-18): 942-53
E. Veron et al., Gallium as a potential candidate for treatment of osteoporosis Drug Discovery Today 2012; 17 (19-20): 1127-32
Acad nat Pharm / Lettre n° 4 déc-2012
ENTREPRISES & BIOTECHS DANS LE DOMAINE DE LA SANTÉ
GENFIT, des biomarqueurs pour le diabète (Création 1999, CA 7,63 millions d'euros)
GENFIT a pour vocation de développer des solutions thérapeutiques et diagnostiques innovantes pour la
prévention et le traitement du diabète et de ses désordres associés. GENFIT déploie une chaîne complète de
compétences allant de la découverte de nouvelles cibles thérapeutiques ou de candidats biomarqueurs jusqu'aux
essais cliniques de Phase II.
A travers un ensemble d'approches complémentaires portant sur le diagnostic précoce, la prévention et le
traitement de ces désordres, GENFIT a développé un pipeline riche et diversifié de blockbusters potentiels en
phase de développement préclinique et clinique, et de cibles thérapeutiques innovantes qui seront à la base de
futurs médicaments « first-in-class ». Ayant pour objet l'identification de nouvelles cibles impliquées dans le
basculement du prédiabète vers le diabète de type 2 et de marqueurs biologiques précoces de ce basculement, ce
programme a permis de financer la construction d'un plan d'études cliniques longitudinales de grande
envergure. Celui-ci a progressé de façon très significative en 2010 avec le démarrage de deux essais cliniques
majeurs. Parmi ceux-ci, le plus avancé est le GFT505 qui cible en particulier plusieurs facteurs de risques du
prédiabète et du diabète : l'hyperglycémie et la résistance à l'insuline, la dyslipidémie athérogène (faible taux de
« Bon Cholestérol » HDL-C, taux élevé de triglycérides) et l'inflammation ainsi que certaines atteintes
hépatiques souvent associées aux états prédiabétiques et diabétiques : la stéatose hépatique non alcoolique
(Non-Alcoholic Fatty Liver Disease ou NAFLD) et l'hépatite stéatosique (Non- Alcoholic Steato-Hepatitis ou
NASH). La FDA vient de donner le feu vert pour le développement clinique en phase IIb de GFT505 aux États-
Source : http://www.france-biotech.org/tag/genfit/
EFFIMUNE depuis 2011, anciennement TCL Pharma. Création 2002 ; test prédisant le rejet des greffes. Spin off
de l'unité INSERM U 643 de Nantes. Nombreuses publications scientifiques de haut niveau. Spécialités les
maladies auto-immunes. Trois produits sont en développement.
Available
Application
Current approach
molecule
molecules
"First in Class"
FR104 (CMO Lonza)
blocking MoAb (memory) Lymphoblastic
depletion Ulcerative
Selective AID (RA,
Anti-p40 MoAb (target Rodent model + 32 Candidate MoAb
Source : http://www.effimune.com, consulté le 21 novembre 2012
IMMUNID (Mesure de l'état du système immunitaire).
Création 2005, CA 450 000 euros, Grenoble, PME 30 personnes
Avec Cytheris, une compagnie biopharmaceutique parisienne fondée sur le développement de facteurs de
croissance capables de stimuler, conduire et restaurer les fonctions du système immunitaire. ImmunID
Acad nat Pharm / Lettre n° 4 déc-2012
Technologies et le Centre Léon Bérard ont annoncé le début de DivRescue, une collaboration en R&D, projet
financée principalement par le 11e appel FUI pour des projets (fonds Interministériels). Le projet DivRescue
vise à développer un nouveau protocole pour la gestion de patients atteints de cancer, évaluer leur état
immunitaire et, lorsque nécessaire, stimuler la reconstitution immunitaire (interleukine 7 recombinante). Cette
première mondiale en théranostique s'appuie sur la synergie entre les trois principaux acteurs : sociétés de
biotechnologie deux Technologies ImmunID et Cytheris - chefs de file en immunologie, de diagnostics et de
pharmacie - et le Centre Léon Bérard (J.-Y. Blay). En priorité : cancer du sein métastatique et cancers solides
ImmunID a également introduit en 2010 un nouveau biomarqueur, la Divpénie®, pouvant rendre compte de
l'étendue des défenses immunitaires d'une personne, au-delà de la simple numération lymphocytaire, ce qui a
contribué à la formulation du concept de la Divpénie®, définie comme un état clinique de diversité
lymphocytaire réduite, facteur pronostique d'un risque accru d'infection et de mortalité
Sources : http:// www.minatec-entreprises.fr/170-IMMUNID, consulté le 15 décembre 2012
http://www.lyonbiopole.com/Actualites/Cytheris-ImmunID-Technologies.html, consulté le 20 décembre 2012
STAGO
La mission première de la division Recherche & Développement (R&D) du Groupe Stago est de concevoir des
produits et solutions (automates, réactifs, consommables, services…) répondant aux besoins des biologistes et
des cliniciens ; l'objectif étant d'améliorer la prise en charge des troubles de l'hémostase et de la thrombose.
Le dernier né de la gamme d'analyseurs Stago, le STA Compact Max®, a été développé par la référence en
STA®-Rivaroxaban Calibrator &Control est une nouvelle solution pour la mesure de la concentration en
rivaroxaban lorsqu'elle est nécessaire. Incluant des calibrants et des contrôles, cette solution utilise une
méthode Anti-Xa (STA®-Liquid Anti-Xa) insensible aux variables analytiques et biologiques et ayant une large
L'Asserachrom® VWF:FVIIIB est l'unique test disponible sur le marché pour mesurer la capacité de liaison du
facteur Von Willebrand au FVIII plasmatique de manière quantitative.
Source : http://www. stago.fr
Acad nat Pharm/ Lettre n° 4 déc-2012 8 /8
Source: http://www.academie-pharmacie.fr/dos_public/Lettre_n-_4_CM_(PSP)_pour_site_public_JPC_27.12.2012.pdf
ANALYSIS OF CARBOHYDRATES AND GLYCOCONJUGATESBY MATRIX-ASSISTED LASER DESORPTION/IONIZATION MASSSPECTROMETRY: AN UPDATE FOR THE PERIOD 2005–2006 David J. Harvey*Department of Biochemistry, Oxford Glycobiology Institute,University of Oxford, Oxford OX1 3QU, UK Received 01 December 2008; received (revised) 26 June 2009; accepted 13 July 2009 Published online 10 March 2010 in Wiley Online Library (wileyonlinelibrary.com). DOI 10.1002/mas.20265
VpCI® Lithium EP Bio-Based Premium Food Machinery Lubri- Corrosion Inhibitor Heavy Duty Grease CorrLube™ VpCI® Lithium EP Lubricant: VpCI®-369 EcoLine® Heavy Duty Grease is EcoLine® Food Machinery Lubricat- Grease is a lithium complex grease formulated with American-grown ing Grease is a high-quality, corrosion formulated with a premium quality, VpCI®-369 is our best inhibitor


